 
| パトリック・O・ブラウン |
 |
|
 |
 |
 |
|
[図 11]

[図 12]

[図 13]
|
[図 11]
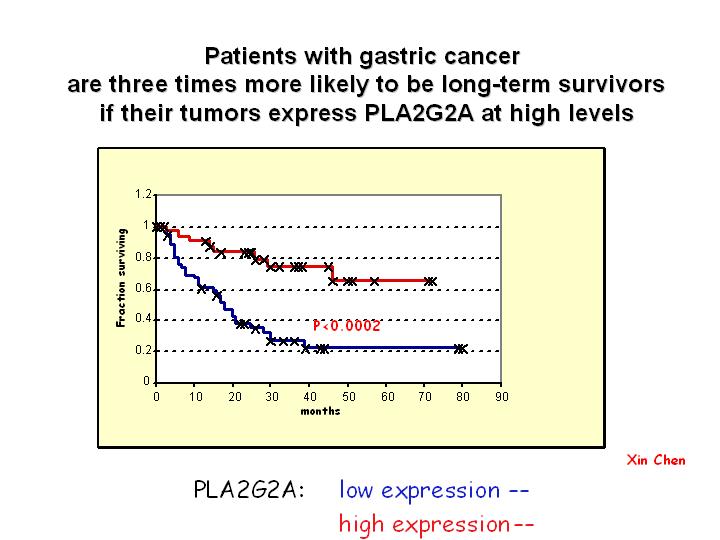
対象となる遺伝子を慎重に探すのも一つの方法です。つまり、ある種のがんにおいて生物学的および臨床的に重要な性質と関連して発現している遺伝子の探索です。これは、私たちが胃がん研究に採用した方法で、患者の生存率を探索の指標にしました。探索の結果、発現パターンが患者の生存率とパラレルな関係にある遺伝子の一つは、PLA2グループ2Aというホスホリパーゼの遺伝子でした。この遺伝子が、腫瘍を除去した後の患者の生存率と深く関係していることを見つけたのです。
私たちは、胃がん患者を二つのグループに分けました。その遺伝子が非常に強く発現しているグループと、発現の弱い(その発現強度の差は2,000倍以上異なる)グループです。そこで私たちが見つけたことは、この酵素を3倍以上も多く発現している患者は、発現の弱い患者より、5年あるいはそれ以上も長生きするということでした。実際に、発現が低いレベルにある患者の80パーセントは、手術後4年までに死亡していますが、この酵素を多く発現していた患者の3分の2は6年経過後も生存していました。
私たちは、この遺伝子については、以前から興味がありました。なぜなら、マウスがもつ同種の遺伝子が、マウスのある特定の腸の腫瘍を軽減する働きをしていることが、数年前に報告されていたからです。このことは、この遺伝子が腫瘍制御遺伝子である可能性を示唆しています。
この遺伝子をさらに興味深くさせているのは、この酵素の生化学的性質がよく知られているからです。つまり、私たちの実験結果は、胃がん患者を救うことができる可能性も示唆しているのです。
まずは、単に、この遺伝子の発現を測定するだけで良いのです。発現レベルの高い患者は、治癒の可能性が高いグループに、それ以外の患者は、より集中的な治療が必要なグループに属すると考えます。
[図 12]
先に述べたように、その酵素の生化学的性質によって、この酵素がどのようにして胃がんの進行を抑制しているのかを知る手がかりが得られます。すなわち、この酵素の防御作用は、この酵素に細胞膜からアラキドン酸を放出する作用があることと関係しているのではないかということです。アラキドン酸は、がん細胞において、プログラム細胞死の過程を活性化することがあります。もし、そのメカニズムが、PLA2グループ2Aの防御作用に関連しているとすれば、直ぐにも治療に利用できる魅力的な方法があります。毒性の低いアスピリンや非ステロイド系の抗炎症剤(NSAID)などの薬は、すでに一般に広く使われていますが、それらの薬は、アラキドン酸をプロスタグランジンなどの誘導体へと代謝するシクロオキシゲナーゼを阻害します。そこで、こうした薬を用いて、アラキドン酸のレベルを上げるという方法が考えられます。
この方法に関しては、アスピリンやNSAIDを服用しているリウマチ患者などには、大腸がんや胃がんになる確率が著しく低いという疫学的な証拠もあって興味深いのですが、これは、酵素作用モデルを支持するものです。
二番目に魅力的な治療方法は、次の事実に由来します。つまり、このホスホリパーゼA2という酵素は、ヒトゲノムにコードされている15個のPLA2の中でも、特に強力な抗菌作用を持っているという特徴があります。つまり、細菌が胃がんを引き起こす原因になることはよく知られていますが、それに加えて、胃がんの進行にも何らかの役割を持っている可能性が浮上しているのです。
以上に述べたモデルは二つとも、胃がん患者の、特にPLA2活性の低い患者の治療にまったく毒性のない治療を施せる可能性を示唆するという点で、興味深いものがあります。この非常に安定な酵素そのものを経口投与することも可能でしょうし、アスピリンやNSAIDでも良いでしょう。また、抗菌作用モデルが正しいとすれば、第三の治療方法として、抗生物質療法が可能かもしれません。もちろん、これらは単なるアイデアにすぎませんので、さらなる研究が必要なのは言うまでもありません。
[図 13]
マイクロアレイ技術が広く利用されるようになってから、まだ10年にもなりませんので、その応用範囲を拡大する試みも始まったばかりです。スティーブは、このテクノロジーの多彩な応用面について、見事な見解を述べましたので、私は、このテクノロジーが近い将来どのように使われるようになるかということを、少しだけ付け加えたいと思います。
私がまず最初に申し上げたいことは、ヒトゲノムの発現プログラムのことや、それが私たちの体にある細胞のタイプと機能に多様性をもたらす仕組みを、私たちは今、探索し始めたばかりだということです。ここ数年のうちに、この種の基礎的な生物学的研究からの情報が急激に増加するのではないかと思います。
二番目の意見は、ここ数年のうちに、がんなどの病気の診断に、DNAマイクロアレイを利用して遺伝子発現プロファイルを調べる方法が、実際に臨床に応用され始めるのではないかということです。すでに、非常に多くの研究が、この方向で進められています。分子標的治療の進展に伴って、この診断法は個別治療の重要な柱になると考えます。
これまで話す機会はなかったのですが、DNAマイクロアレイを使うことで大きな発展を遂げようとしている分野があります。そこでは、環境、すなわち、海、河川、土壌などの変化をモニターしたり調査したりします。そうした変化は、人間活動によって、また、自然現象や気候変動などによって起こりますが、それらの環境にもとから棲んでいる微生物などを観測対象にします。
他には、プロテオミクスの分野でマイクロアレイが頻繁に使われることになると思います。つまり、細胞内や、血液や尿などの体液中にあるタンパク質の変異や変化を調べるためです。がんのような病気を調べるために、血液試験のような臨床試験方法を開発しようと、多大な努力がなされています。
|
|
|