 
| パトリック・O・ブラウン |
 |
|
 |
 |
 |
|
[図 8]
[図 9]

[図 10]
|
そこで、このようなマップを使って、特徴的な表現の仕方をする一連の遺伝子が、機能的に近い関係にあるというような、遺伝子の相互関係を調べたり、分子レベルで共通の性質をもつ生体サンプル同士の、あるいは種々の細胞同士や組織間の違いを見分けたり、細胞や組織サンプルの特徴と特定の遺伝子を関連づけたりします。
たとえば、ミトコンドリアで発現し、酸素呼吸に関係するこれら一連の遺伝子の発現レベルを見ることによって、明るい黄色で示された組織、すなわち、心臓、骨格筋、腎臓、脳の酸素要求度が最高レベルにあることを予測できます。
細胞分裂サイクルのプロセスに関係する遺伝子を詳しく調べることによって、分裂速度が速い細胞や組織を同定することもできます。
また、雄だけでしか発現しない遺伝子を調べれば、細胞や組織のなかで、どれが男性に由来し、どれが女性に由来するかを見分けることができます。
遺伝子発現パターンから得られる情報には、こうしたサンプルの分子的生物的形質のようなもの以外にも数多くありますので、このようなマップを、生物学的特性を示す標準の図として使って遺伝子発現パターンを解読することができるのです。
[図 8]
ところで、スティーブの話にもあったように、世界中で多くの科学者が、ヒトの病気、特にがんにおける遺伝子発現パターンを調べるために、DNAマイクロアレイを使って研究しています。
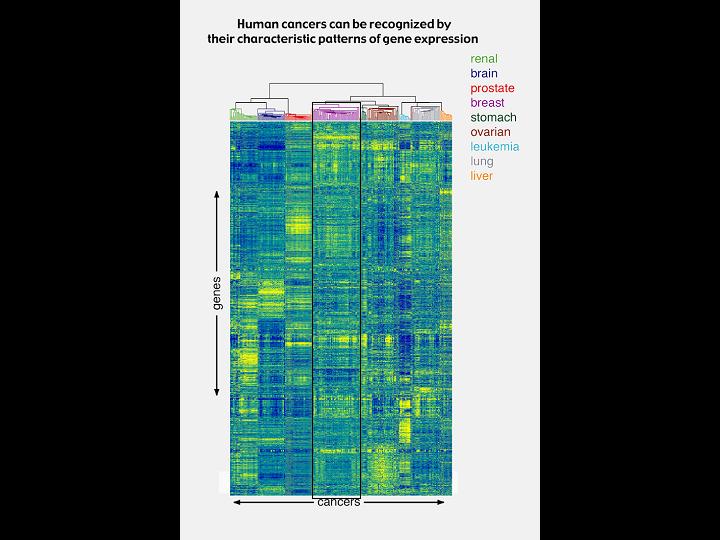
このマップは、先程示したものとよく似ていますが、数百人のがん患者から採取した様々ながんの遺伝子発現パターンをまとめたものです。
このマップの一番上に描かれたツリー構造は、腫瘍の発現パターンにおける類似性を表していますが、従来の診断方法に従って、それを個々のがんに色分けしました。ここからわかることの一つは、その遺伝子発現パターンによって、乳がん、前立腺がん、脳腫瘍、腎がんなどを簡単に見分けることができるということです。それぞれのがんは、がんの種類によって、その細胞の性質に違いをもたらす遺伝子発現パターンがあるのです。また、がんサンプル全ての遺伝子発現パターンが正常な体の組織と違うことも容易に区別することができます。
こうしたパターンから、これらのがん一つ一つにおける生理的機能や分子レベルでの制御について多くの情報を得ることができます。正常な組織と比較すれば、ある種の腫瘍でだけ選択的に発現される遺伝子が、直ちにわかります。その遺伝子を標的とする分子は、標的治療薬に適用できるかもしれません。新しい分子標的薬は、現在開発中のものもありますし、臨床試験段階にあるものもありますが、こうした薬剤とともに、この種の分析も、患者一人一人に対応する個別治療の重要な要素になることでしょう。
正常な体組織とそれぞれのがんに特有な分子レベルにおけるパターンを同定すれば、それらのパターンは、初期のがんを発見するための新たなスクリーニング法や診断テストへの第一歩となります。
DNAマイクロアレイががん研究に貢献したことのなかで、最も重要なことの一つは、遺伝子発現プログラムに基づいた新たながんの分類法と診断法を進展させたことでした。二、三の例を見てみましょう。
乳がんは、他のがんと簡単に区別できると言いましたが、よく見ると、乳がん全てが同じというわけではなく、個々の患者の腫瘍は、その遺伝子発現パターンにおいても個々に異なります。
私たちは、長い間、顕微鏡のもとで同じに見える乳がんなら、同じ乳がん患者として分類してきました。ところが、患者固有の臨床経過があり、治療に対しても患者固有の反応を示すことがわかったのです。今では、反応性の違いを左右すると考えられる分子レベルでの相違を見つけだすことも可能です。以前には見分けのつかなかったがんで、遺伝子発現プログラムに基づいたがんのサブタイプが定義されると、そこから治療に対する反応や臨床経過の違いを予測できるわけですが、実際に、これからは、こうした例が次々と見つかるでしょう。
[図 9]
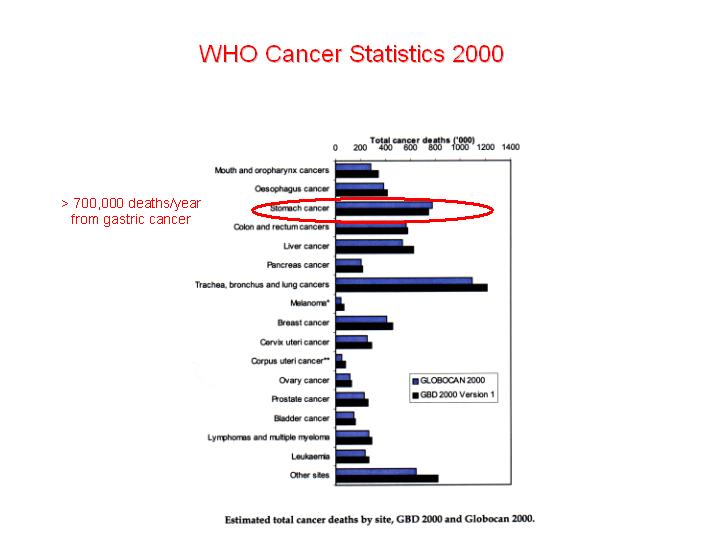
では、どのようにしてこのアプローチをがん研究に利用すればよいのかを、ちょっとした例をあげて説明しようと思います。それは胃がんに関するものです。皆さんもご存知のように、胃がんは、日本で特に重要な医学的問題ですが、世界でも、がんとしては2番目の死因になっています。
[図 10]
私の研究室のポスドクである、シン・チェンと、共同研究者のレウン、ユエン、サム・ソー達は、DNAマイクロアレイを使って、胃がん患者からの腫瘍サンプル100個以上の遺伝子発現プロファイルを作成しました。このマップを見てもわかるように、個々のサンプルにおける遺伝子発現パターンは、すべて異なっています。つまり、同じがんをもつ患者は一人としていなかったのです。実に、それらは驚くべき多様性を示していました。
私たちがもっているデータの中には、こうした腫瘍の分子レベルでの特徴を示す有用な情報が膨大にありますが、これ程多くの違いがあっては、どこに焦点を当てたら良いのかわからなくなります。研究に最も必要な情報となるような特定の遺伝子を、どうやって選べばよいのでしょうか。
|
|
|